Cannabinoïden

Hoe worden nieuwe cannabinoïden ontdekt en inge...
De wetenschap heeft een enorme verschuiving doorgemaakt, van een tijd waarin slechts enkele cannabinoïden bekend waren tot nu, aan de rand van een nieuw onderzoeksgebied. In mijn professionele loopbaan binnen...
Hoe worden nieuwe cannabinoïden ontdekt en inge...
De wetenschap heeft een enorme verschuiving doorgemaakt, van een tijd waarin slechts enkele cannabinoïden bekend waren tot nu, aan de rand van een nieuw onderzoeksgebied. In mijn professionele loopbaan binnen...

Hoe verschillen synthetische cannabinoïden van ...
Het gesprek rond synthetische en plantaardige cannabinoïden wordt steeds relevanter. Synthetische cannabinoïden worden in laboratoria ontwikkeld om met specifieke receptoren in het lichaam te interageren. Hun gerichte ontwerp brengt eigenschappen...
Hoe verschillen synthetische cannabinoïden van ...
Het gesprek rond synthetische en plantaardige cannabinoïden wordt steeds relevanter. Synthetische cannabinoïden worden in laboratoria ontwikkeld om met specifieke receptoren in het lichaam te interageren. Hun gerichte ontwerp brengt eigenschappen...
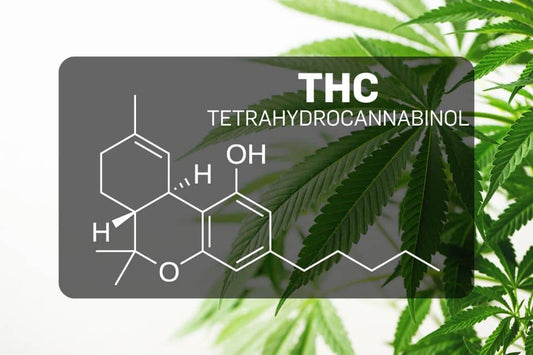
Wat is THC (Tetrahydrocannabinol)?
THC, of tetrahydrocannabinol, is de bekendste psychoactieve stof in de cannabisplant en staat vooral bekend om het gevoel dat vaak wordt omschreven als 'high'. Nu de interesse in cannabis toeneemt,...
Wat is THC (Tetrahydrocannabinol)?
THC, of tetrahydrocannabinol, is de bekendste psychoactieve stof in de cannabisplant en staat vooral bekend om het gevoel dat vaak wordt omschreven als 'high'. Nu de interesse in cannabis toeneemt,...

De geschiedenis van THC
THC, ook bekend als tetrahydrocannabinol, is de belangrijkste psychoactieve stof die wordt aangetroffen in de cannabisplant. Met een geschiedenis die duizenden jaren teruggaat, is cannabis door mensen gebruikt voor zowel...
De geschiedenis van THC
THC, ook bekend als tetrahydrocannabinol, is de belangrijkste psychoactieve stof die wordt aangetroffen in de cannabisplant. Met een geschiedenis die duizenden jaren teruggaat, is cannabis door mensen gebruikt voor zowel...

Welke cannabinoïden veroorzaken een psychoactie...
De psychoactieve werking van cannabis wordt vooral toegeschreven aan specifieke cannabinoïden in de plant. Deze cannabinoïden interageren met het endocannabinoïdesysteem van het lichaam, wat verschillende effecten heeft op stemming, waarneming...
Welke cannabinoïden veroorzaken een psychoactie...
De psychoactieve werking van cannabis wordt vooral toegeschreven aan specifieke cannabinoïden in de plant. Deze cannabinoïden interageren met het endocannabinoïdesysteem van het lichaam, wat verschillende effecten heeft op stemming, waarneming...

Wat zijn cannabinoïden?
Inleiding tot Cannabinoïden Cannabinoïden zijn een groep actieve verbindingen die in de cannabisplant worden gevonden. Deze van nature voorkomende stoffen zijn verantwoordelijk voor veel van de effecten van cannabis, van...
Wat zijn cannabinoïden?
Inleiding tot Cannabinoïden Cannabinoïden zijn een groep actieve verbindingen die in de cannabisplant worden gevonden. Deze van nature voorkomende stoffen zijn verantwoordelijk voor veel van de effecten van cannabis, van...

Wat is CBN (Cannabinol)?
CBN, kort voor cannabinol, verschijnt in cannabis wanneer THC begint af te breken. Het komt slechts in kleine hoeveelheden voor en is niet zo krachtig als THC, maar speelt nog...
Wat is CBN (Cannabinol)?
CBN, kort voor cannabinol, verschijnt in cannabis wanneer THC begint af te breken. Het komt slechts in kleine hoeveelheden voor en is niet zo krachtig als THC, maar speelt nog...

Wat is CBG (cannabigerol)?
CBG, kort voor cannabigerol, krijgt steeds meer aandacht in het cannabinoïdeonderzoek vanwege zijn unieke rol binnen de cannabisplant. In tegenstelling tot THC is CBG niet bedwelmend en veroorzaakt het geen...
Wat is CBG (cannabigerol)?
CBG, kort voor cannabigerol, krijgt steeds meer aandacht in het cannabinoïdeonderzoek vanwege zijn unieke rol binnen de cannabisplant. In tegenstelling tot THC is CBG niet bedwelmend en veroorzaakt het geen...

Wat is HHC (Hexahydrocannabinol)?
Gedurende mijn carrière heb ik verschillende verbindingen binnen de cannabisplant bestudeerd, en vandaag richt ik mijn aandacht op een stof die de laatste tijd veel belangstelling heeft gekregen: hexahydrocannabinol, of...
Wat is HHC (Hexahydrocannabinol)?
Gedurende mijn carrière heb ik verschillende verbindingen binnen de cannabisplant bestudeerd, en vandaag richt ik mijn aandacht op een stof die de laatste tijd veel belangstelling heeft gekregen: hexahydrocannabinol, of...

Wat is CBD (Cannabidiol)?
CBD (cannabidiol) is een van de meest onderzochte cannabinoïden uit de cannabisplant. Het staat bekend om zijn onderscheidende eigenschappen ten opzichte van THC, aangezien CBD geen psychoactieve effecten veroorzaakt en...
Wat is CBD (Cannabidiol)?
CBD (cannabidiol) is een van de meest onderzochte cannabinoïden uit de cannabisplant. Het staat bekend om zijn onderscheidende eigenschappen ten opzichte van THC, aangezien CBD geen psychoactieve effecten veroorzaakt en...

Wat is CBC (Cannabichromeen)?
Onder de verbindingen in Cannabis sativa L. is er één cannabinoïde die steeds meer belangstelling wekt: cannabichromeen, oftewel CBC. CBC werd voor het eerst geïdentificeerd in 1966 en komt langzaam...
Wat is CBC (Cannabichromeen)?
Onder de verbindingen in Cannabis sativa L. is er één cannabinoïde die steeds meer belangstelling wekt: cannabichromeen, oftewel CBC. CBC werd voor het eerst geïdentificeerd in 1966 en komt langzaam...

Wat is het entourage-effect bij cannabis?
Het Entourage Effect: Een uitgebreide gids Cannabis kent een lange geschiedenis van gebruik, zowel in traditionele contexten als voor recreatieve doeleinden. Pas in de 20e eeuw begonnen wetenschappers systematisch te...
Wat is het entourage-effect bij cannabis?
Het Entourage Effect: Een uitgebreide gids Cannabis kent een lange geschiedenis van gebruik, zowel in traditionele contexten als voor recreatieve doeleinden. Pas in de 20e eeuw begonnen wetenschappers systematisch te...

Wat zijn 2-AG en anandamide?
In mijn recente jaren in de CBD sector en bij Formula Swiss heb ik mij intensief beziggehouden met de studie van cannabinoïden en hun relatie tot natuurlijke processen in het...
Wat zijn 2-AG en anandamide?
In mijn recente jaren in de CBD sector en bij Formula Swiss heb ik mij intensief beziggehouden met de studie van cannabinoïden en hun relatie tot natuurlijke processen in het...

Wat is CBGV (Cannabigerivarine)?
Hoewel CBD en THC nog steeds de meeste aandacht krijgen in gesprekken over cannabinoïden, begint cannabigerivarine (CBGV) steeds meer op te vallen vanwege zijn unieke structuur en toenemende aanwezigheid in...
Wat is CBGV (Cannabigerivarine)?
Hoewel CBD en THC nog steeds de meeste aandacht krijgen in gesprekken over cannabinoïden, begint cannabigerivarine (CBGV) steeds meer op te vallen vanwege zijn unieke structuur en toenemende aanwezigheid in...
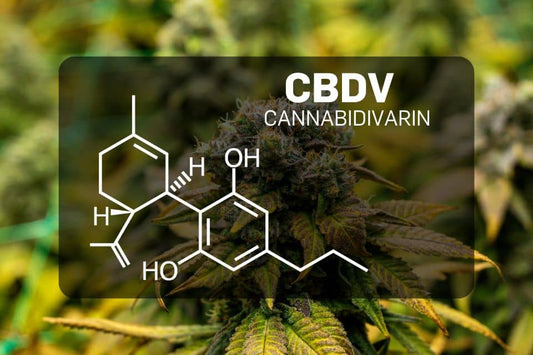
CBDV - Cannabidivarine
CBDV, of cannabidivarine, is een niet-bedwelmende cannabinoïde die van nature voorkomt in bepaalde soorten Cannabis sativa. Het is nauw verwant aan CBD, maar heeft een iets andere chemische structuur die...
CBDV - Cannabidivarine
CBDV, of cannabidivarine, is een niet-bedwelmende cannabinoïde die van nature voorkomt in bepaalde soorten Cannabis sativa. Het is nauw verwant aan CBD, maar heeft een iets andere chemische structuur die...
